Dosage de l'acide phosphorique
discipline : physique-chimie
Le but: évaluer la quantité d’acide phosphorique contenue dans le coca cola pour voir si elle respecte la norme des 0,6 g/L.
Il faut tout d’abords décolorer le soda afin d’être en mesure de voir les changements de couleurs lors du dosage.
Situation: nous somme partis à la Faculté Des Sciences à l'aide de M.Tabyaoui et M.Talbaoui pour réaliser cette expérience.
Matériel :
- 2 béchers de 100 mL
- 100 mL de boisson dégazée (on a dégazé nos boissons en laissant le bouchon ouvert une semaine puis 30 minutes avec un agitateur magnétique pour être sur qu’il ne restait aucune trace de dioxyde de carbone)
- Du charbon actif
- 1 entonnoir
- 1 papier filtre
- 1 agitateur en verre
- 1 spatule
Protocole expérimental :
¬ Mesurer 100mL de boisson
¬ Verser environ 3 à 4 cuillères de charbon actif dans la boisson à l’aide d’une spatule
¬ Remuer la solution avec l’agitateur
¬ Laisser reposer une dizaine de minutes
¬ Filtrer la solution en rajoutant du charbon actif dans l’entonnoir
On obtient ainsi, une boisson totalement décolorée.
Nous allons donc doser la boisson (Coca Cola) avec de la Soude de concentration à 0.02 mol.L-1 par Titrage pH-métrique
Matériel :
- 50 mL de soude de concentration 0.02 mol.L-1
- 20mL de boisson dégazée (la nôtre sera décolorée, mais cela n’a pas d’importance pour notre expérience puisque nous ne faisons pas un dosage à l’équivalence avec un indicateur pH)
- 1 bécher de 100 mL
- 1 pissette d’eau distillée Pipette jaugée de 20 mL munie de son système d’aspiration
- Une burette graduée
- Agitateur magnétique muni de son barreau aimanté
- pH-mètre
Protocole expérimental :
¬ Prélever 20 ml de boisson à l’aide d’une pipette jaugé, puis verser dans un bécher de 100mL
¬ Ajouter dans ce bécher 20mL d’eau distillée dans ce même bécher mesurés à l’aide d’une pipette jaugé
¬ Introduire dans le bécher le barreau aimanté
¬ Placer le bécher sur l’agitateur magnétique
¬ Rincer l’électrode du pH mètre avec de l’eau distillée (afin de nettoyer l’électrode et d’obtenir un maximum de précision lors du titrage)
¬ Mettre sous tension l’agitateur magnétique.
¬ Une fois la solution correctement mélangée. Arrêter l’agitateur magnétique.
¬ Introduire l’électrode du pH-mètre dans le bécher
¬ Mettre sous tension le pH-mètre
¬ Relever la valeur initiale de pH et la reporter dans un tableau
¬ Ajouter 1mL de soude dans le bécher à l’aide de la burette graduée
¬ Remettre sous tension l’agitateur magnétique
¬ L’arrêter
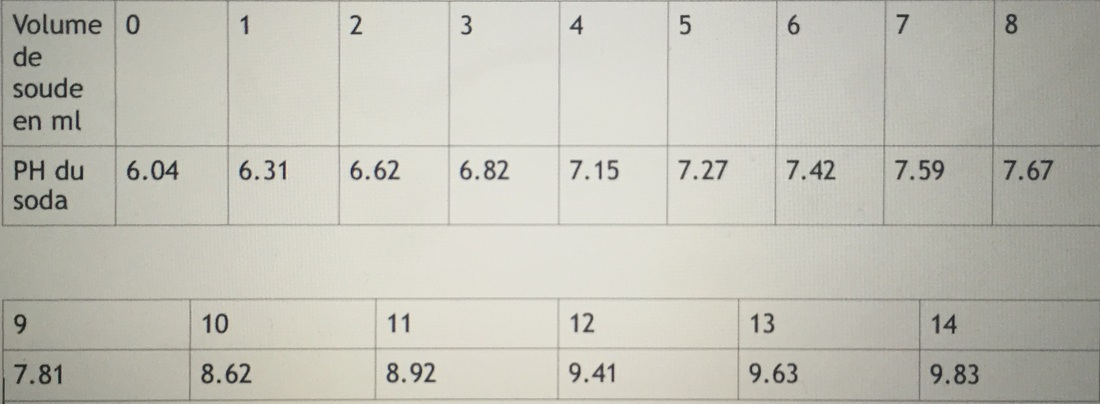
¬ Lire le pH, reporter sa valeur dans le tableau
Continuer le dosage en complétant le tableau au fur et à mesurer jusqu’à V=14mL de soude (ce volume devrait être suffisant pour obtenir une solution basique pH=9).
Il faut tout d’abords décolorer le soda afin d’être en mesure de voir les changements de couleurs lors du dosage.
Situation: nous somme partis à la Faculté Des Sciences à l'aide de M.Tabyaoui et M.Talbaoui pour réaliser cette expérience.
Matériel :
- 2 béchers de 100 mL
- 100 mL de boisson dégazée (on a dégazé nos boissons en laissant le bouchon ouvert une semaine puis 30 minutes avec un agitateur magnétique pour être sur qu’il ne restait aucune trace de dioxyde de carbone)
- Du charbon actif
- 1 entonnoir
- 1 papier filtre
- 1 agitateur en verre
- 1 spatule
Protocole expérimental :
¬ Mesurer 100mL de boisson
¬ Verser environ 3 à 4 cuillères de charbon actif dans la boisson à l’aide d’une spatule
¬ Remuer la solution avec l’agitateur
¬ Laisser reposer une dizaine de minutes
¬ Filtrer la solution en rajoutant du charbon actif dans l’entonnoir
On obtient ainsi, une boisson totalement décolorée.
Nous allons donc doser la boisson (Coca Cola) avec de la Soude de concentration à 0.02 mol.L-1 par Titrage pH-métrique
Matériel :
- 50 mL de soude de concentration 0.02 mol.L-1
- 20mL de boisson dégazée (la nôtre sera décolorée, mais cela n’a pas d’importance pour notre expérience puisque nous ne faisons pas un dosage à l’équivalence avec un indicateur pH)
- 1 bécher de 100 mL
- 1 pissette d’eau distillée Pipette jaugée de 20 mL munie de son système d’aspiration
- Une burette graduée
- Agitateur magnétique muni de son barreau aimanté
- pH-mètre
Protocole expérimental :
¬ Prélever 20 ml de boisson à l’aide d’une pipette jaugé, puis verser dans un bécher de 100mL
¬ Ajouter dans ce bécher 20mL d’eau distillée dans ce même bécher mesurés à l’aide d’une pipette jaugé
¬ Introduire dans le bécher le barreau aimanté
¬ Placer le bécher sur l’agitateur magnétique
¬ Rincer l’électrode du pH mètre avec de l’eau distillée (afin de nettoyer l’électrode et d’obtenir un maximum de précision lors du titrage)
¬ Mettre sous tension l’agitateur magnétique.
¬ Une fois la solution correctement mélangée. Arrêter l’agitateur magnétique.
¬ Introduire l’électrode du pH-mètre dans le bécher
¬ Mettre sous tension le pH-mètre
¬ Relever la valeur initiale de pH et la reporter dans un tableau
¬ Ajouter 1mL de soude dans le bécher à l’aide de la burette graduée
¬ Remettre sous tension l’agitateur magnétique
¬ L’arrêter
¬ Lire le pH, reporter sa valeur dans le tableau
Continuer le dosage en complétant le tableau au fur et à mesurer jusqu’à V=14mL de soude (ce volume devrait être suffisant pour obtenir une solution basique pH=9).
Ainsi, on retrouve donc le volume équivalent au premier saut de pH, nous en avons conclu qu’il s’agissait du premier pour l’acide phosphorique. Après avoir tracé les tangentes, on retrouve le volume équivalent de soude pour chaque boisson VéqCoca-cola: : 8.4mL.
L’acide possède 3 groupes carboxyles (COOH) qui peuvent céder chacun 1 proton lors d’une réaction acido-basique (celui qui capte ces protons est appelé base l’autre qui les libère est appelé acide d’où le nom de la réaction noté sous la forme
Acide = base + H), d’où 3 protons libérés par la molécule. L’acide citrique est donc un triacide. Le terme triacide signifie que 1 mol d’acide phosphorique libère 3 mol de protons. Chaque proton se fixe sur un ion hydroxyde et donc il faut 3 mol d’ions hydroxyde pour une mole d’acide phosphorique. La réaction acido-basique avec l’acide-phosphorique correspond à :
OH- + H+ H2O
H3PO4 PO4³- + 3H+
Calcul de la concentration massique d’acide citrique dans le Coca-Cola light : On sait que : Csoude = 2,0.10-2 mol.L-1 ;
Véq= 8,4mL = 9,7.10-3 L ; VCoca-Cola =2.0.10-2 L
C acide =(V soude X C soude) / 3 x V Boisson
C acide = 2.28 x 10-3 mol.L-1
On sait que la masse molaire M de l’acide phosphorique est de 93 g/mol
Donc Cm= 2.28 x 10-3 mol.L-1 X 98 = 0.29 g/L
On peut conclure que le coca cola respecte la norme fixée.
L’acide possède 3 groupes carboxyles (COOH) qui peuvent céder chacun 1 proton lors d’une réaction acido-basique (celui qui capte ces protons est appelé base l’autre qui les libère est appelé acide d’où le nom de la réaction noté sous la forme
Acide = base + H), d’où 3 protons libérés par la molécule. L’acide citrique est donc un triacide. Le terme triacide signifie que 1 mol d’acide phosphorique libère 3 mol de protons. Chaque proton se fixe sur un ion hydroxyde et donc il faut 3 mol d’ions hydroxyde pour une mole d’acide phosphorique. La réaction acido-basique avec l’acide-phosphorique correspond à :
OH- + H+ H2O
H3PO4 PO4³- + 3H+
Calcul de la concentration massique d’acide citrique dans le Coca-Cola light : On sait que : Csoude = 2,0.10-2 mol.L-1 ;
Véq= 8,4mL = 9,7.10-3 L ; VCoca-Cola =2.0.10-2 L
C acide =(V soude X C soude) / 3 x V Boisson
C acide = 2.28 x 10-3 mol.L-1
On sait que la masse molaire M de l’acide phosphorique est de 93 g/mol
Donc Cm= 2.28 x 10-3 mol.L-1 X 98 = 0.29 g/L
On peut conclure que le coca cola respecte la norme fixée.